“美国FDA对国外药物进入本土市场的监管重视程度有增无减,是否可以免除I期、II期临床取决于研究数据质量、产品的安全性和临床数据过硬。康柏西普获得美国FDA批准,直接进入III期,说明已经具备了完整的药物有效性和安全性数据。”
——前美国FDA高级评审官魏晓雄博士表示
近日康弘药业研发的朗沐(康柏西普眼用注射液)获准在美国开展III期临床试验,引发行业对于中国创新医药的讨论。究竟直接进入美国FDA(食品药品监督管理局)III期临床意味着什么?中国医药企业在通向FDA的道路上又“遭遇”着怎样的严苛考验?
全球“通关”名额不足20个
统计数据显示,通过FDA认证的新药,平均开发成本是10亿美元,耗时10年以上,成功的概率大约是1/6000。
放眼国内,通过美国食品与药品监督管理局(FDA)审批并由此进军世界主流医药市场一直是中国医药企业的目标和梦想,药品通过FDA上市是一个极其严格的过程,每年美国FDA批准上市的新药不超过20个,能够直接进入临床III期者,放眼世界寥寥无几。
因此,将康弘朗沐的“连跳两级” 斩获“FDA III期批准手续”称为中国制药史上里程碑式的胜利,绝非过誉。
解读康柏西普“连跳两级”
康柏西普创造的奇迹在于,由于其设计、研发、生产,研究的最高质量标准,不需要在美进行I期、II期的临床试验,直接进入III期临床,这对中国原研的创新药物国际化之路,将是历史性的时刻。
朗沐(康柏西普)是中国医药工业历史上第一个直接进入美国FDAIII期临床研究的创新药,也是中国第一个获得FDA临床批件(IND)的中国生物药。朗沐,堪称国家重大创制专项标识化成果之一。
此次跳级,康弘朗沐(康柏西普)将有望更加快速的进入世界医药第一大市场——美国,进而更广阔的天地,在全球范围内改变跨国公司垄断湿性年龄相关性黄斑变性(wAMD)治疗的格局。
当美国人选择中国创造,你的选择是什么?
“洋药”、“国药”的观念之争持续多年,创新和质量标准一度让“洋药”引以为傲,“国药”真的不及“洋药”吗?对于国药与洋药的PK,四川的李成(化名)先生有着切身体会,一年前在得知患有后,李成第一时间到美国进行治疗,多次赴美踏破铁鞋而收效甚微,经过多方咨询,最终在国内华西医院专家的推荐下,使用康柏西普(朗沐)得到了更经济、有效的治疗。
还有一个患者,来自海外的Aaron(化名)在充分了解病症治疗方案后,不远万里来到中国,选择用康柏西普治疗眼底黄斑水肿(如图)。如同Aaron选择康柏西普,未来的国际市场上会有更多的人选择“中国创造”。
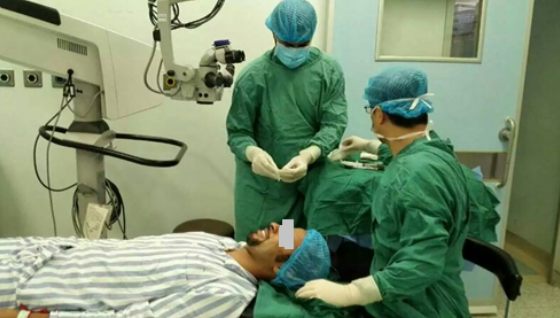
对于国人而言,此次美国FDA批准康弘朗沐“连跳两级”,是对国药创新能力、技术领先水平极有力的证明,在眼科领域黄斑变性的治疗上,国人可以不再“崇洋”。
医药界的“十年一剑”
中国“制造大国”现象的一大憾事,在于众多企业放弃对“至精至微”的追求,“十年磨一剑”的轶事逐渐久远。
然而探寻康弘朗沐的成功之路发现,十年前康弘药业朗沐(康柏西普)启动研发,累计投入超10亿,同时将国际最高质量标准的要求贯穿从研发到生产到上市销售的每一个环节。朗沐的研发阵容采用国际专家联合中国专家的实力组合,上市两年时间,迅速得到市场的广泛认可,在国内市场率先打破跨国企业的强势垄断。
同时,朗沐的国际化之路自它诞生之时便开始了,回顾上市以来,多项康柏西普的临床研究结果,先后被第12届美国新生血管年会、2015美国眼科年会、2015年美国视网膜专家学会年会等全球性的眼科会议邀请做专题报道,为朗沐在国际市场上建立了良好的口碑和信誉。
中国加入WTO组织已经十余年,对于入世影响最大的三个产业之一的医药行业,同各国高手在一个竞争平台上同舞了十余年。而今,在康弘朗沐这一民族品牌上,我们终于可以调转观念,见证创新药“中国创造”的国际风采!






暂无评论
要发表评论,您必须先 登录